病理报告是了解肿瘤病人病情最重要的也是最直接的资料,同时也是指导病人后续治疗的重要依据。 ·III级就是晚期了吗? ·免疫组化是什么? ·各个英文指标是什么意义? 各个医院病理检测报告可能呈现上不一样,但是内容上大同小异,一般分为肉眼所见及病理诊断两大部分。 肉眼所见:该部分主要是标本的外观描述及取材包埋处理方法,一般无需过多关注。 其中最重要的信息是乳腺包块/结节的大小,如“外象限见一结节,大小2*1.5*1.2cm,切面灰白质韧界欠清”、“剖面见一灰白灰黄色质稍实区域,直径2.5cm”等类似描述,该指标有助于肿瘤T分期。 病理诊断:一般分为两个部分,分别是: 1.常规染色阅片结果(报告上文字描述部分) 2.免疫组化结果(报告上用各英文简写指标描述) 今天我们先讲讲文字描述部分。 组织学类型 “浸润性癌,非特殊类型”是乳腺癌最常见的病理类型。 浸润性癌指癌组织突破基底膜向间质发生浸润。 一般来说,浸润性癌在手术后还需要进一步的治疗,但具体的治疗方案还需根据患者整体病情及免疫组化结果(见后)决定。 与之相对应的概念就是“原位癌”,原位癌即病变没有突破基底膜,没有发生浸润。 通常我们比喻原位癌为“襁褓中的婴儿”,才出生不久,暂时没有能力到处跑(转移可能性极小),同时也易于控制(治疗)。 而“非特殊类型”则相对于“特殊类型”而言。 特殊类型的乳腺癌的报告方式常为:浸润性癌+特殊癌名称。 常见的特殊类型的乳腺癌有: 浸润性小叶癌、黏液癌、伴大汗腺分化的癌、化生性癌、微乳头状癌、囊腺癌等。 组织学分级是针对浸润性癌的进一步描述,根据是否有腺管形成、细胞核多形性及核分裂象计数3项指标进行分级,建议采用Nottingham分级系统,每项1-3分,共9分。 总分为3~5分,组织学分级为Ⅰ级 总分为6~7分,组织学分级为Ⅱ级 总分为8~9分,组织学分级为Ⅲ级 组织学分级是肿瘤细胞生长活跃度的一种体现,不能代表肿瘤分期。 很多病人或家属看到“Ⅲ级8分”“Ⅲ级9分”就以为是肿瘤晚期了,这种想法显然是错误的! 所以千万不要自己吓自己哟!组织学分级
脉管侵犯
脉管通常指血管和淋巴管,脉管侵犯或浸润是复发转移的高危因素之一。
肿瘤切缘状态(阳性或阴性)
切缘报告一般针对保乳手术而言。
在保乳手术中,因需保证手术切缘阴性,所以常规对切缘行术中冰冻(快速病理)检查。
部分肿瘤侵犯皮肤的局部晚期患者术中也会根据情况看是否需要行皮肤切缘病理检查,确定切除范围是否足够。
乳头,皮肤,胸肌筋膜等是否见癌累及
指在显微镜下看特殊部位是否有癌细胞浸润,可作为病理分期的依据之一。
淋巴结见/未见癌转移(n/N)
一般N代表一共的淋巴结个数,n代表在检测的淋巴结中阳性的个数。
淋巴结转移与否同样是乳腺癌复发转移的高危因素之一。
前哨淋巴结指肿瘤转移的第一站,若前哨淋巴结阴性,则肿瘤转移至更远处的可能性就较低。
在乳腺癌手术中,前哨淋巴结的快速冰冻活检结果决定了手术中是否清扫腋窝淋巴结。
若前哨淋巴结阳性则需清扫腋窝淋巴结,若前哨淋巴结阴性,则保留腋窝淋巴结,这是为了提高患者术后的生活质量。
MP(Miller-Payne)分级
该指标是针对新辅助治疗(先化疗和/或靶向治疗后再行手术)标本的,不同分级代表肿瘤对前期治疗的反应程度。
一般分为5级,分级越高表明药物治疗效果越好。
通常认为MP 5级等同于病理完全缓解(pCR),研究表明该部分病人的预后优于相同分期分级先手术后化疗的病人。
免疫组化全称是免疫组织化学技术(immunohistochemistry),是应用免疫学基本原理——抗原抗体反应。
即抗原与抗体特异性结合的原理,通过化学反应使标记抗体的显色剂显色来确定组织细胞内抗原(多肽和蛋白质),对其进行定位、定性及相对定量的研究。
整个操作过程步骤复杂,时间较长。
若你的医生让你等免疫组化结果,请一定耐心等待。
免疫组化可以帮助病理医生进行鉴别诊断从而更加明确病理诊断,同时可以明确乳腺癌分子类型、指导治疗(化疗,靶向治疗、内分泌治疗)并提示预后。
免疫组化的指标很多,临床医生一般最关注以下四个:
ER—雌激素受体(Estrogen Receptor)
PR—孕激素受体(Progesterone Receptor)
这两项性激素受体决定着患者是否为激素依赖性乳腺癌,是否可以进行内分泌治疗。
常见的表达方式为:
ER(-)
ER(+)(强,阳性率约70%)
PR(+)(中等强度,阳性率约60%)
其中+表示为阳性,可以进行内分泌治疗;
显示-表示为阴性,暂无指证应用内分泌治疗;
而表达百分比越高、表达程度越强,则提示内分泌治疗效果可能越好。
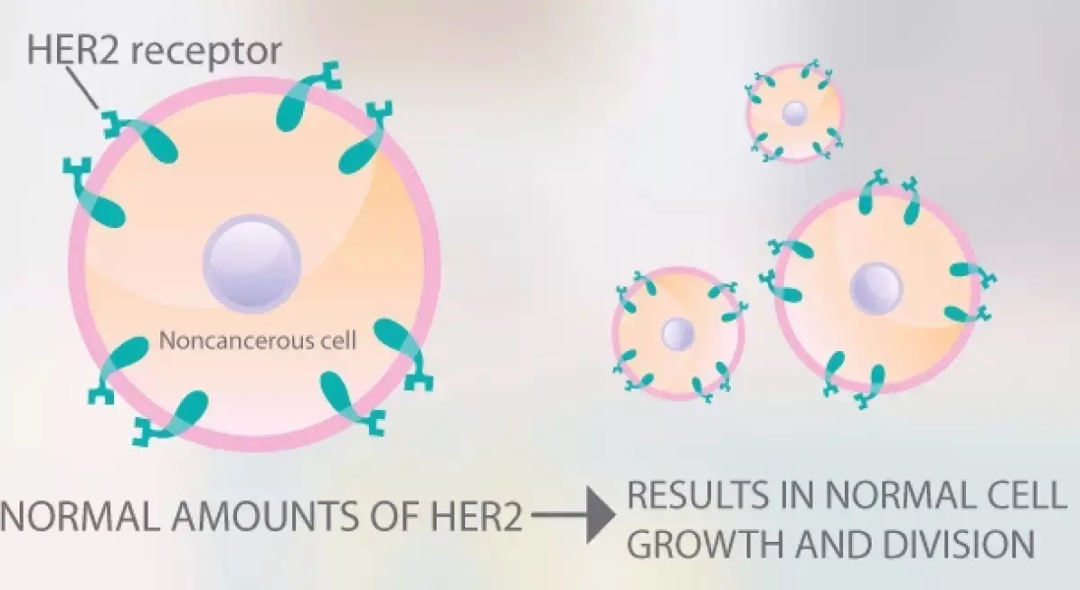
HER2:人表皮生长因子受体2

人表皮生长因子受体家族包括4位成员——HER1、HER2、HER3和HER4,乳腺癌细胞中表达最多的就是HER2。
作为跨膜蛋白,它们可以在细胞表面与生长因子结合,进行信号传导,调节细胞的生长、分裂和修复。
正常状态下,HER基因处于非激活状态。
HER2表达与否决定了是否可以进行靶向治疗,若为阳性,则需要使用曲妥珠单抗、帕妥珠单抗等抗HER2的靶向治疗药物,如果为阴性,则该类药物无效。
病理报告中常见的表达方式为:
HER2(-)
HER2(1+)
HER2(2+)
HER2(3+)
与ER、PR的解读不同,这里不能看到“+”就认为是阳性。
其中“-”和“1+”均代表HER2基因表达为阴性,应用抗HER2靶向治疗无效。
若显示“3+”则代表HER2基因表达阳性,可以使用抗HER2靶向治疗。
若显示“2+”则表达单纯的免疫组化尚不能明确其状态,还需要进行FISH(荧光原位杂交,fluorescence in situ hybridization)检测。
若FISH检测提示基因扩增则表示该基因表达可行抗HER2靶向治疗。
Ki-67 是与细胞周期相关的一种核蛋白,是与细胞增殖有关的指标,与肿瘤细胞浸润、转移、种植的能力密切相关。
阳性且表达的百分比越高,意味着肿瘤生长越快,组织分化越差,对化疗也越敏感(是否需要化疗取决于多个因素,如肿瘤大小、肿瘤分期、淋巴结转移情况、分子分型等)。
Ki-67高表达是预后差的危险因素之一。
ER、PR、HER2及Ki-67四项指标决定了乳腺癌的分子分型,并且是药物治疗的重要参考依据。
乳腺癌免疫组化中其他的指标如AR(雄激素受体)、P53/ target=_blank class=infotextkey>P53抑癌基因、E-cadherin(钙粘附蛋白E)、CK5/6(细胞角蛋白5/6)等也与乳腺癌复发、转移、预后有一定相关性,但参考价值不及前述四项指标。